Bài báo này trình bày các kết quả nghiên cứu ảnh hưởng của nhiệt độ, thời gian nung đến sự thay đổi cấu trúc và chất lượng của quặng vê viên được nung ở nhiệt độ (500÷1200) oC trong 2 h.
Effect of induration temperatures on the structure and quality of Narua-Caobang iron ore pellets
NGUYỄN THANH HOÀN*, BÙI ANH HÒA, NGUYỄN SƠN LÂM
Viện Khoa học và kỹ thuật vật liệu, Trường Đại học Bách khoa Hà Nội.
*Email: hoancongthuong@gmail.com
Ngày nhận bài: 19/5/2018, Ngày duyệt đăng: 26/7/2018
TÓM TẮT
Bài báo trình bày kết quả nghiên cứu ảnh hưởng của nhiệt độ đến cấu trúc, chất lượng của quặng viên khi được nung trong vùng nhiệt độ từ (500÷1200) °C với thời gian giữ nhiệt (1÷2) h. Quặng sắt Nà Rụa, Cao Bằng dạng bột có kích thước hạt ≤ 0,25 mm trộn chất kết dính 2 % bentonit. Quá trình vê viên được thực hiện với quặng sắt ở độ ẩm 10 % để tạo viên dạng cầu có kích thước (12÷14) mm, sau đó được sấy khô ở nhiệt độ 100 °C trong 2 h. Quặng sắt thay đổi thành phần khoáng vật từ Fe3O4 chuyển thành khoáng vật Fe2O3 khi nung ở nhiệt độ cao từ 900 °C. Sự thay đổi cấu trúc được thể hiện qua sự thay đổi diện tích bề mặt riêng của viên quặng là 3,469 m2/g ở nhiệt độ 500 °C giảm xuống 0,119 m2/g khi ở nhiệt độ 1200 °C trong 2 h. Thể tích riêng của lỗ trống của quặng viên giảm từ 0,009 cm3/g xuống 0,001 cm3/g khi được nung tương ứng ở 500 và 1200 °C trong 2 h. Nhiệt độ và thời gian giữ nhiệt đã làm thay đổi tính chất và cấu trúc của viên quặng vê viên, đáp ứng chất lượng của quá trình hoàn nguyên.
Từ khóa: vê viên, quặng viên, Fe2O3, Fe3O4.
ABSTRACT
The effect of temperature and holding time on the structure and quality of iron ore pellets was investigated. The pellets are heated at a temperature range of (500÷1200) °C for 1 and 2 h. Narua-Caobang iron oxides with a par- ticle size below 0.25 mm were mixed with 2 % fine bentonite as binder material. The pelleting process is carried out with a moisture of 10 % using disk pelletizer machine to prepare pellets of (12÷14) mm in diameter. The green pellets were dried at 100 °C for 2 h. Iron ore pellets changed mineral composition from Fe3O4 to Fe2O3 when heat- ed at high temperature from 900 °C. The structure changes of the pellets can be indentified via the change in the specific surface area from 3.469 m2/g at the induration temperature of 500 °C down to 0.119 m2/g at the induration temperature of 1200 °C. The specific porous volume of pellets is reduced from 0.009 cm3/g to 0.001 cm3/g when heated at 500 and 1200 °C for 2 h, respectively. The temperature and time of induration process changed the struc- ture and quality of the pellets, which control of the quality of the reduction process.
Keywords: pelleting, iron ore pellets, Fe2O3, Fe3O4.
1. ĐẶT VẤN ĐỀ
Vê viên là quá trình tạo ra vật liệu kích thước nhất định từ quặng sắt dạng bột, tang quay hoặc đĩa quay được dùng để tạo viên quặng có dung dịch thấm ướt (H2O) và chất kết dính. Quặng vê viên được sử dụng cho mục đích luyện gang lò cao hoặc luyện sắt xốp [1-7]. Để đáp ứng yêu cầu cần thiết cho việc sử dụng, quặng vê viên được nung ở nhiệt độ thấp hơn nhiệt độ thiêu kết 1300°C để đảm bảo độ bền, độ xốp và tính luyện kim được tốt hơn [8]. Khi nghiên cứu về quặng vê viên Tekkalakote Umadevi cùng các cộng sự [9] đã đưa ra nhiệt độ tối ưu là 1220 °C và kích thước quặng vê viên là 14 mm có tính hoàn nguyên tốt nhất. Các tính chất về hoàn nguyên của quặng vê viên đã được Liu, Kumar và Ettabirou [3, 10, 11] đưa ra trong bài toán nhiệt động học, ảnh hưởng của chất kết dính, chất hoàn nguyên đến tốc độ cũng như mức độ hoàn nguyên của quặng vê viên cũng được đề cập.
Bài báo này trình bày các kết quả nghiên cứu ảnh hưởng của nhiệt độ, thời gian nung đến sự thay đổi cấu trúc và chất lượng của quặng vê viên được nung ở nhiệt độ (500÷1200) oC trong 2 h.
2. THỰC NGHIỆM
Quặng sắt được lấy từ mỏ sắt Nà Rụa – Cao Bằng, nhờ máy nghiền kiểu đĩa tạo hạt có kích thước ≤ 0,25 mm. Mẫu quặng sắt dạng bột được phân tích thành phần khoáng vật bằng phương pháp nhiễu xạ Rơnghen trên thiết bị D8 – Advance, sử dụng bức xạ Cu, kết quả được nêu trong bảng 1.
Bảng 1. Thành phần khoáng vật trong mẫu quặng sắt ban đầu (% khối lượng)
| Khoáng vật | Hàm lượng (%) |
| Manhetit – Fe3O4 | 58 – 60 |
| Hematit – Fe2O3 | 20 – 21 |
| Gơtit – Fe2O3.H2O | 6 – 8 |
| Quartz – SiO2 | 7 – 9 |
Quặng bột sau khi nghiền phân cấp được phối trộn với 2 % bentonit làm chất kết dính và phun sương tạo ẩm 10 %. Đã sử dụng máy vê viên kiểu đĩa để tạo viên quặng dạng cầu đường kính (12÷14) mm.
Các mẫu viên quặng sau khi vê viên đạt kích thước được đưa vào lò nung điện cực SiC với tốc độ tăng nhiệt là 10 °C/phút tại các chế độ khác nhau: 500 oC, 1 h; 900 oC, 1000 oC, 1100 oC và 1200 oC, giữ nhiệt trong 1 và 2 h.
Thành phần pha các mẫu quặng viên sau nung ở các nhiệt độ và thời gian khác nhau được phân tích nhiễu xạ Rơnghen dùng bức xạ Cu Kα (λ = 1,54059 Å); góc quét: 20-80°; bước quét: 0,03; thời gian mỗi bước: 0,8 s. Hình thái học bề mặt và thành phần nguyên tố được phân tích trên thiết bị hiển vi điện tử quét phát xạ trường JSM-7600F, JEOL. Đặc tính nhiệt của mẫu được phân tích trên thiết bị phân tích nhiệt-trọng lượng và phân tích nhiệt vi sai (TG/DTA) với tốc độ nâng nhiệt 10 K/phút trong môi trường khí Ar.
Để đánh giá sự thay đổi cấu trúc của quặng viên được nung ở nhiệt độ khác nhau và thời gian là 2 h đã xác định diện tích bề mặt, thể tích và bán kính lỗ trống bằng phương pháp đo hấp phụ trên thiết bị Autosorb iQ, và phương pháp phân tích BET sử dụng N2 lỏng.
Phương pháp đo độ bền nén được tiến hành theo quy định YB/T 5166-1993 của Hiệp hội Gang thép Trung Quốc, hiện đang được áp dụng tại các nhà máy sản xuất gang ở Việt Nam.
3. KẾT QUẢ VÀ THẢO LUẬN
Tính chất của quặng viên phụ thuộc vào trạng thái nhiệt hóa như nhiệt độ nung và thời gian giữ nhiệt do các phản ứng nhiệt-hóa, tái kết tinh và sự hình thành pha xỉ. Pha xỉ hình thành quanh viên quặng và di chuyển vào tâm viên quặng trong quá trình nung rắn. Pha xỉ được thiêu kết mật độ cao làm cầu nối liên kết tăng độ bền của viên quặng.
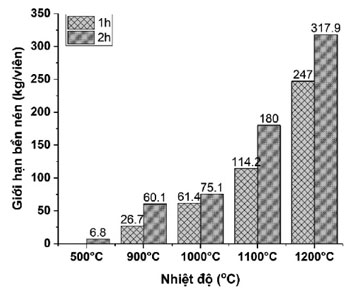
Độ bền nén của viên quặng sắt vê viên sau khi được nung oxi hóa được trình bày tại hình 1. Độ bền quặng viên thiêu trong 1 h tại các nhiệt độ 900, 1000, 1100 và 1200 °C tương ứng là 26,7; 61,4; 114,2 và 247 kg/viên sẽ tăng lên khi nung thiêu 2 h tại các nhiệt độ 900, 1000, 1100 và 1200°C tương ứng là 60,1; 75,1; 180 và 317,9 kg/viên. Sự gia tăng độ bền nén khi tăng nhiệt độ và thời gian nung thiêu là do chất kết dính chảy lỏng và làm chảy các hạt quặng, làm tăng độ bền của quặng viên nung thiêu [12]. Mẫu viên quặng được nung ở nhiệt độ 1200 °C với thời gian giữ nhiệt trong 2 h đã đạt được cơ tính lớn nhất với độ bền nén trung bình của viên đạt 317,9 kg/viên, kết quả này thỏa mãn được yêu cầu nguyên liệu cho quá trình luyện gang lò cao là ≥ 250 kg/viên [6, 12].
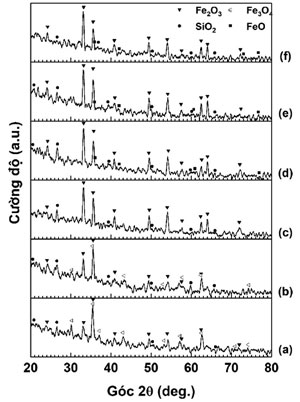
Hình 2 cho kết quả phân tích nhiễu xạ Rơnghen của các mẫu quặng viên ban đầu và nung thiêu oxy hóa tại 500, 900, 1000, 1100 và 1200 °C trong 2 h. Thành phần khoáng vật các mẫu viên quặng sau khi nung thiêu thiêu ở các nhiệt độ và thời gian giữ nhiệt được xác định từ giản đồ nhiễu xạ Rơnghen được liệt kê trong bảng 2.
Bảng 2. Thành phần khoáng vật của mẫu quặng viên sau khi nung
| Chế độ nung | Thành phần khoáng vật và khoảng hàm lượng (%) | ||||
| Hematit Fe2O3 |
Manhetit Fe3O4 |
Vutit FeO | Thạch anh | Khoáng vật khác | |
| 500 °C, 2h | 20 ÷ 21 | 58 ÷ 60 | – | 7 ÷ 9 | – |
| 900 °C, 1h | 89 ÷ 91 | – | 6 ÷ 8 | Clorit | |
| 900 °C, 2h | 89 ÷ 91 | – | 4 ÷ 6 | – | |
| 1000 °C, 1h | 91 ÷ 93 | – | 2 ÷ 4 | – | |
| 1000 °C, 2h | 88 ÷ 90 | 3 ÷ 5 | 2 ÷ 4 | – | |
| 1100 °C, 1h | 90 ÷ 92 | 3 ÷ 5 | 1 ÷ 3 | – | |
| 1100 °C, 2h | 90 ÷ 92 | 3 ÷ 5 | 1 ÷ 3 | – | |
| 1200 °C, 1h | 90 ÷ 92 | 3 ÷ 5 | 1 ÷ 3 | – | |
| 1200 °C, 2h | 91 ÷ 93 | 3 ÷ 5 | 1 ÷ 3 | – | |
Kết quả phân tích bằng phương pháp nhiễu xạ Rơnghen đã cho thấy quặng viên có thành phần khoáng vật ban đầu phần lớn là manhetit (Fe3O4) và một phần là hematit (Fe2O3). Quá trình chuyển biến đối với quặng cầu viên sau khi được thực hiện ở nhiệt độ 1200 °C với thời gian giữ nhiệt trong 2 h được giải thích bởi các yếu tố như:
– Khi nung ở nhiệt độ cao trong môi trường oxy hóa hạt quặng manhêtít sẽ bắt đầu oxy hóa, tạo mầm vi tinh thể Fe2O3 và lớn lên, hình thành cầu nối liên kết các hạt lại. Khi nung ở nhiệt độ 900 °C, hình thức liên kết đó có thể làm cho cường độ của quặng cầu viên tăng lên. Nhưng do nhiệt độ thấp, sự lớn lên của vi tinh thể Fe2O3 rất hạn chế, vì vậy liên kết này cho độ bền của cầu viên không đủ sử dụng làm nguyên liệu cho lò cao do chỉ đạt độ bền nén 60,1 kg/viên.
– Quá trình kết tinh lại Fe2O3 được thực hiện khi quặng cầu viên được nung ở nhiệt độ lớn hơn 900°C, quá trình chuyển biến hoàn toàn quặng manhetit thành hematit khi thực hiện nung ở nhiệt độ 1000 °C đến 1200 °C. Hematit mới sinh bắt đầu kết tinh lại và lớn lên trở thành tinh thể quặng hematit liên kết chặt với nhau, làm cho viên cầu có độ bền cao. Kết quả đo độ bền nén tại hình 1 đã cho thấy sự tăng lên và đạt mức cao khi thực hiện mẫu đo tại 1200 °C với thời gian giữ nhiệt trong 2 h.
Bảng 3 là kết quả đo diện tích bề mặt riêng, thể tích riêng và bán kính lỗ trống.
Bảng 3. Kết quả đo mẫu viên quặng bằng phương pháp hấp phụ
| Nhiệt độ (°C) |
Thời gian (phút) |
Diện tích bề mặt riêng (m2/g) |
Thể tích riêng lỗ trống (cm3/g) |
Bán kính lỗ trống (Å) |
| 500 | 120 | 3,469 | 0,009 | 19,175 |
| 900 | 120 | 1,671 | 0,007 | 38,870 |
| 1000 | 120 | 0,313 | 0,001 | 21,308 |
| 1100 | 120 | 0,118 | 0,001 | 18,899 |
| 1200 | 120 | 0,119 | 0,001 | 16,872 |
Bảng 3 cho thấy sự phân tán và độ rỗng của viên quặng ở nhiệt độ 500 °C có thể tích lỗ trống là 0,009 cm3/g và bán kính lỗ trống 19,175 Å. Trong giai đoạn đầu khi nung thiêu từ 500 lên 900°C, có thể đã xuất hiện các nứt vi mô từ quá trình chuyển biến cấu trúc tinh thể giữa pha ban đầu là manhetit (cấu trúc spinel lập phương) và pha mới hình thành hematit (cấu trúc sáu phương xếp chặt). Quá trình này cũng làm phát triển nhanh nứt vi mô và sự lớn lên của các mầm êmatít dẫn đến bán kính lỗ trống tăng lên đến 38,870 Å. Do sự dịch chuyển xảy ra mãnh liệt ở nhiệt độ cao (từ 1000 đến 1200 °C) đã làm cho thể tích lỗ trống trong viên quặng cầu viên dần dần được lấp đầy, các hạt tinh thể nhỏ tụ tập hình thành hạt tinh thể lớn hơn và tạo thành các phiến lớn, đây chính là nguyên lý của quá trình phản ứng pha rắn. Độ rỗng của viên quặng ở nhiệt độ 1200 °C có thể tích lỗ trống là 0,001 cm3/g và bán kính lỗ trống 16,872Å, kết quả này gần với quặng tự nhiên theo nghiên cứu hoàn nguyên quặng hematit của Jianwen Yu [13]. Sự hình thành các hỗn hợp cùng tinh trong quá trình nung oxy hóa viên quặng ở nhiệt độ cao trong phản ứng pha rắn như các chất: FeO; FeO- SiO2; CaO.SiO2 đã làm tăng độ bền của quặng cầu viên đạt 317,9 kg/viên tại nhiệt độ 1200 °C với thời gian giữ nhiệt 2 h.

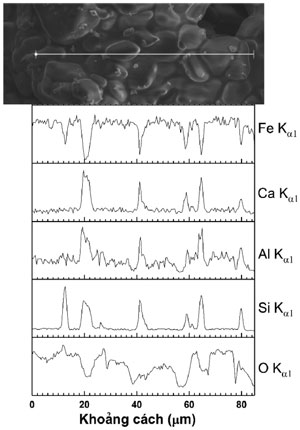
Ảnh hiển vi điện tử quét của viên quặng được nung oxy hóa tại nhiệt độ 1200 °C trong 2 h được trình bày trên hình 3. Trong viên quặng các hạt quặng oxit sắt đều có dạng góc tù tại các đầu mút. Điều này được giải thích là do sự lớn lên của Fe2O3 trong quá trình kết tinh lại hay sự hình thành các hỗn hợp cùng tinh trong quá trình nung oxy hóa viên quặng ở nhiệt độ cao. Giản đồ phổ phân tán năng lượng (hình 4) cho thấy kích thước của các hạt quặng khoảng ≤ 20 m và sự hình thành các pha thông qua sự phân bố của các nguyên tố Fe, O, Si, Ca và Al. Bao quanh biên hạt các hạt oxit sắt là các pha xỉ có chứa các oxit của Si, Ca và Al. Các pha xỉ là cầu nối dính kết tốt với các hạt oxit sắt tạo mẫu quặng vê viên có độ bền cao [14].
Phương pháp phân tích nhiệt vi sai và phân tích nhiệt-trọng lượng được sử dụng để kiểm tra mẫu quặng sắt Nà Rụa nhằm xác định nhiệt độ chuyển pha, xác định khối lượng mất đi trong quá trình chuyển pha. Phương pháp phân tích nhiệt dựa trên việc thay đổi nhiệt độ của mẫu đo. Đối với mẫu đo thì luôn xẩy ra một trong hai hiện tượng giải phóng (tỏa nhiệt) và hấp phụ nhiệt (thu nhiệt) khi tăng nhiệt độ của hệ, tùy thuộc vào trạng thái chuyển pha tương ứng, kèm theo là sự thay đổi nhiệt độ và trọng lượng theo nhiệt độ. Từ đó có thể xác định được nhiệt độ chuyển pha đối với mẫu viên quặng sắt nghiên cứu.
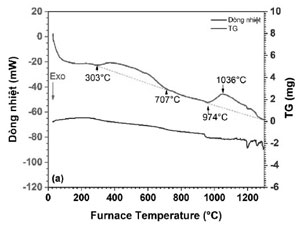
Kết quả kiểm tra TG/DTA mẫu quặng sắt Nà Rụa được trình bày tại giản đồ hình 5 khi nung từ nhiệt độ phòng đến 1300 °C, tốc độ nâng nhiệt độ 10 °C/phút, trong khí Ar. Giản đồ DTA cho thấy có 2 píc thu nhiệt ở khoảng nhiệt độ (303÷707) °C và (974÷1300) °C. Píc thu nhiệt thứ nhất có thể do các quá trình bay hơi nước, chuyển pha rắn- lỏng… Tuy nhiên các quá trình này diễn ra chậm, có thể nhận thấy đường phân tích nhiệt-trọng lượng có độ dốc thoai thoải và đi xuống. Về đặc tính, quặng hematit có hai biến thể là α-hematit (cấu trúc lục giác thường thấy) and γ-hematit (cấu trúc lập phương; chỉ tạo thành ở dưới (400÷500) °C) [15]. Tùy thuộc nguồn gốc quặng và hàm lượng ion ngoại lai, γ-hematit chuyển biến sang α-hematit trong khoảng nhiệt độ (370÷600) °C và quá trình này là thu nhiệt. Bên cạnh sự chuyển biến từ γ-hematit sang α-hematit, trong thành phần quặng còn có một lượng lớn ẩm dính hóa học (gơtit Fe2O3.H2O) được giải phóng hoàn toàn ở nhiệt độ khoảng 500 °C. Trong khoảng nhiệt độ 200 đến 450 °C, các nghiên cứu cho thấy có các phản ứng phân hủy hyđrat và khử ẩm dính từ gơtit sang hematit như sau:
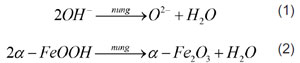
Píc thu nhiệt thứ 2, đặc trưng trong khoảng nhiệt độ (974÷1300) °C, tương ứng với sự hóa hơi của kim loại kiềm và chảy lỏng của xỉ với đỉnh chảy lỏng ở 1036 °C. Khối lượng giảm mạnh tại nhiệt độ 974 °C trên đường TG do chất bốc hoặc kim loại kiềm bay hơi. Tại khoảng nhiệt độ này cũng có thể xuất hiện các chuyển pha như sự phân hủy CaCO3 [16] và phân hủy của hematit thành manhetit:
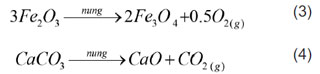
4. KẾT LUẬN
– Quặng sắt manhetit Nà Rụa Cao Bằng có kích thước ≤ 0,25 mm được tạo viên dạng cầu có đường kính (12÷14) mm sau khi sấy vào nung oxy hóa ở nhiệt độ từ 500 đến 1200 °C với thời gian giữ nhiệt trong 1 h và 2 h, ở nhiệt độ trên 900 °C đã chuyển hóa hoàn toàn thành hematit (Fe2O3).
– Mẫu nung thiêu 1200 °C, 2 h cho thấy bán kính lỗ trống là 16,872 Å với thể tích riêng là 0,001 cm3/g; và hình thái hạt quặng có dạng góc tù tròn đầu, pha oxit Si, Ca và Al tập trung tại biên hạt quặng, tạo thành cầu nối liên tục giữa pha xỉ và oxit sắt.
– Phân tích DTA mẫu quặng sắt manhetit ban đầu cho thấy píc nhiệt thứ 2 tại 974 đến 1300 °C cho thấy các quá trình chuyển biến của các pha oxit của Si, Ca và Al đã thúc đẩy sự hình thành các cầu nối làm tăng độ bền quặng viên.
– Quặng viên nung thiêu 1200 °C, 2 h đã đạt được cơ tính lớn nhất với độ bền nén 317,9 kg/viên, thỏa mãn yêu cầu công nghiệp của nguyên liệu phục vụ cho quá trình luyện gang lò cao.
TÀI LIỆU TRÍCH DẪN
- R.C. Gupta, Theory and laboratory experiments in ferrous metallurgy, New Delhi-110001: PHI Learning Privated Limited, 2010.
- Ahindra Ghosh and Amit Chatterjee; Ironmaking and steelmaking: theory and practice, New Delhi-110001: PHI Learning Privated Limited, 2008.
- Mithilesh Kumar, Himanshu Baghel, and Saroj Kumar Patel; Reduction and Swelling of Fired Hematite Iron Ore Pellets by Non-coking Coal Fines for Application in Sponge Ironmaking, Mineral Processing and Extractive Metallurgy Review, 34(4), 2013, p. 249-267.
- H. U. Ross, The Fundamental Aspects of Iron Ore Reduction, in Symposium on Science and Technology of Sponge Iron and Its Conversion to Steel, 1973: CSIR – National Metallurgical Laboratory, Jamshedpur.
- J. R. Wynnyckyj and T. Z. Fahidy; Solid state sintering in the induration of iron ore pellets, Metallurgical Transactions, 5(5), 1974, p. 991-1000.
- Bodil E. Monsen, Edith S. Thomassen, Irene Bragstad, Eli Ringdalen, and Per H. Hoegaas; Characterization of DR Pellets for DRI Applications, in AISTech 2015 Proceedings O. AISTech 2015, Proceedings At: Cleveland, Ohio, USA.
- D. Zhu, J. Pan, L. Lu, and R. J. Holmes; 15 – Iron ore pelletization, in Iron Ore, L. Lu (Editor), Woodhead Publishing, 2015, p. 435-473.
- Srinivas Dwarapudi, T. Uma Devi, S. Mohan Rao, and Madhu Ranjan; Influence of Pellet Size on Quality and Microstructure of Iron Ore Pellets, ISIJ International, 48(6), 2008, p. 768-776.
- Tekkalakote Umadevi, Naveen Frank Lobo, Sangamesh Desai, Pradipta Chandra Mahapatra, RameshwarSah, and Manjunath Prabhu; Optimization of Firing Temperature for Hematite Pellets, ISIJ International, 53(9), 2013, p. 1673-1682.
- Gui-su Liu, Vladimir Strezov, John A. Lucas, and Louis J. Wibberley; Thermal investigations of direct iron ore reduction with coal, Thermochimica Acta, 410(1), 2004, p. 133-140.
- Mohamed Ettabirou, Bernard Dupré, and Charles Gleitzer; Hematite ore reduction to magnetite with CO/CO2 – kinetics and microstructure, Steel Research, 57(7), 1986, p. 306-311.
- Kotta Anand Babu, Karak Swapan Kumar, and M. Kumar; Characterization of iron ore pellets with dextrin added organic binders under different time and temperature conditions, IOP Conference Series: Materials Science and Engineering, 178(1), 2017, p. 012003.
- Jianwen Yu, Yuexin Han, Yanjun Li, Peng Gao, and Wenbo Li; Mechanism and Kinetics of the Reduction of Hematite to Magnetite with CO-CO2 in a Micro-Fluidized Bed, Minerals, 7(11), 2017.
- Jagannath Pal, Satadal Ghorai, Manik Ch Goswami, Sukomal Ghosh, Dinabandhu Ghosh, and Debajyoti Bandyopadhyay; Development of Fluxed Iron Oxide Pellets Strengthened by CO2 Treatment for Use in Basic Oxygen Steel Making, ISIJ International, 49(2), 2009, p. 210-219.
- Anil Kumar Biswas; Principles of Blast Furnace Ironmaking: Theory and Practice: Cootha, 1981.
- Isabel Galan, Fredrik P. Glasser, and Carmen Andrade; Calcium carbonate decomposition, Journal of Thermal Analysis and Calorimetry, 111(2), 2013, p. 1197-1202.
