Trên cơ sở kết quả phân tích thành phần vật chất của quặng tinh graphit Bảo Hà, đã khảo sát chế độ nung phân hủy quặng tinh…
Material compositions of graphite concentrate from Bao Ha mine and examination roasting of conditions
Đỗ Hồng Nga
Viện Khoa học và Công nghệ Mỏ – Luyện kim
Ngày nhận bài: 22/9/2015, Ngày duyệt đăng: 14/10/2015
Tóm tắt
Trên cơ sở kết quả phân tích thành phần vật chất của quặng tinh graphit Bảo Hà, đã khảo sát chế độ nung phân hủy quặng tinh. Kết quả khảo sát cho thấy, với chế độ công nghệ được lựa chọn, bao gồm: tác nhân phân hủy là NaOH, nhiệt độ: 450 oC, thời gian: 1 giờ và tỷ lệ NaOH/quặng tinh = 1/2, sau đó hòa tách ở chế độ chọn trước như: nồng độ dung môi 10 % H2SO4, thời gian 2 giờ, nhiệt độ thường, tỷ lệ R/L = 1/5. Từ quặng tinh graphit có hàm lượng 83,2 % C có thể nâng lên > 95 % C theo phương pháp hóa ướt.
Abstract
Based on the analysis of material composition of the graphite concentrate from Bao Ha, are examined the roasting conditions for decomposition of graphite concentrate. Experiment all results show, that with the conditions selected, including decomposing agent: sodium hydroxide, the temperature: 450oC, time: 1 hour and of NaOH/graphite concentrate ratio: 1/2, after digestion with: 10 % H2SO4, for 2 hours, at room temperature and solid/liquid ratio: 1/5, the C content can be increased from 83.2 % (graphite concentrate) up to more 95% by wet chemical method.
1. Mở đầu
Graphit là một khoáng mềm, có độ cứng theo thang Mohs từ 0,51 và có khối lượng riêng 2,092,26 g/cm3 [1]. Nó có màu xám sang màu đen, mờ đục và có ánh kim. Ngoài ra, nó có độ dẫn nhiệt và điện cao, đặc biệt trơ về mặt hóa học.
Hiện nay, graphit chất lượng cao được ứng dụng trong nhiều lĩnh vực bao gồm: các hệ thống lưu trữ điện, như các loại pin và các tế bào nhiên liệu, ma sát, chổi than cho động cơ điện, vật liệu chịu lửa, chất bôi trơn và luyện kim.
Graphit gồm 2 loại: tự nhiên và nhân tạo. Graphit tự nhiên được sản xuất từ quặng tinh graphit với hàm lượng và kích thước hạt khác nhau. Graphit nhân tạo được sản xuất chủ yếu từ nguồn cốc dầu mỏ nên hafm lượng có thể đạt tới 99,9% C [2].
Để nhận được graphit độ sạch cao, tùy thuộc vào đặc điểm thành phần vật chất của quặng tinh, có thể sử dụng phương pháp hóa học [3] hoặc phương pháp nhiệt [4], tuy nhiên phương pháp hóa học sử dụng phổ biến hơn cả [5].
Trong khuôn khổ bài báo này, tác giả tập trung nghiên cứu thành phần vật chất của quặng tinh graphit Bảo Hà, từ đó lựa chọn chế độ nung phân hủy phù hợp để xử lý quặng tinh graphit vùng này.
2. Thực nghiệm
Các phương pháp được sử dụng để xác định thành phần vật chất gồm:
Phương pháp phân tích hóa học được sử dụng để xác định thành phần hóa học của các cấu tử tồn tại trong quặng tinh graphit Bảo Hà.
Phương pháp phân tích nhiễu xạ tia Rơnghen để xác định dạng tồn tại của cacbon và các tạp chất. Thiết bị được sử dụng là Siemens D5005, xuất xứ Đức.
Phương pháp phân tích khoáng tướng, thạch học nhằm xác định độ mịn nghiền quặng nguyên khai trên cơ sở kích thước vảy graphit.
Mẫu nghiên cứu là quặng tinh graphit Bảo Hà đã qua quá trình nghiền – tuyển nổi để đạt chất lượng 80-85 %C, ngoài ra còn có các tạp chất như: SiO2, Al2O3, Fe2O3, CaO và MgO.
Thành phần cỡ hạt được trình bày trong bảng 1.
Bảng 1. Thành phần cỡ hạt của quặng tinh graphit Bảo Hà
| Cấp hạt, mm | Phân bố, % |
| -0,177 + 0,1 | 23,00 |
| -0,1 + 0,074 | 4,25 |
| -0,074 | 72,75 |
| Tổng | 100 |
3. Kết quả và thảo luận
3.1. Thành phần hóa học và thành phần khoáng vật
Bằng việc lựa chọn các phương pháp phân tích nêu trên, kết quả thành phần hóa học, thành phần khoáng vật lần lượt được trình bày trong bảng 2 và bảng 3. Giản đồ nhiễu xạ tia rơnghen được nêu trong hình 1. Kết quả phân tích khoáng tướng, thạch học nêu trong hình 2 và 3.
Bảng 2. Thành phần hóa học quặng tinh graphit Bảo Hà, %
| C | Chất bốc | Tro | ẩm | |||
| 83,2 | 1,87 | 14,8 | 0,2 | |||
| Thành phần tro | ||||||
| Al2O3 | SiO2 | Fe2O3 | CaO | MgO | ||
| 11,3 | 30,6 | 29,6 | 6,38 | 2,46 | ||
Bảng 3. Thành phần khoáng vật quặng tinh graphit Bảo Hà
| Tên khoáng vật | Thành phần, % |
| Graphit – T (C) | 84,8 |
| Anorthit (Ca0.7Mg0.3Al2Si2O8) | 7,4 |
| Cohenit (FeC3) | 4,6 |
| Thạch anh (SiO2) | 3,2 |
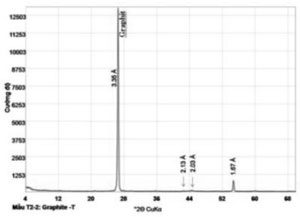
Từ kết quả phân tích thành phần vật chất quặng tinh graphit Bảo Hà cho thấy, graphit tồn tại ở dạng đơn khoáng (83 – 84 % C), còn lại chủ yếu là tro (14,8 %) và chất bốc (1,87 %). Chiếm thành phần nhiều nhất trong tro là SiO2 với hàm lượng 30,6 %, là loại tạp chất khó loại bỏ, nó chỉ hòa tan trong một vài dung môi như: axit HF – là loại axit độc hại, đắt tiền, và kiềm [7].
Trong mẫu quặng nguyên khai, graphit tồn tại dưới dạng tấm dài, vảy hoặc sợi, xâm tán khá dày trong nền mẫu, xen kẹp giữa các tấm phi quặng (thạch anh, mica…), có chỗ sắp xếp thành đám ổ. Các tấm sợi thường có dạng uốn lượn (hình 2) hoặc dạng vảy (hình 3). Ngoài những dạng nêu trên, graphit Bảo Hà còn tồn tại một lượng rất nhỏ dạng kết tinh vô định hình, xâm nhiễm cùng với pyrotin, pyrit và phi quặng.

Như đã trình bày, để loại SiO2 thường chọn NaOH, môi trường này cũng có thể loại được một phần tạp chất Al2O3 có trong quặng tinh graphit.
Các tạp chất khác trong thành phần tro như: Al2O3, Fe2O3, CaO, MgO có hàm lượng nhỏ, để loại bỏ được chúng chỉ cần hòa tan trong môi trường axit. Một số công trình nghiên cứu [5], [7] cho thấy, HCl có tác dụng hòa tan các tạp chất kể trên tốt hơn H2SO4. Tuy nhiên, H2SO4 vẫn ưu tiên được sử dụng do chi phí thấp hơn.
Khi xử lý quặng tinh graphit với kiềm NaOH (hoặc nung chảy kiềm với quặng tinh hoặc hòa tách quặng tinh trong autocla) [8] nếu có mặt SiO2 sẽ xảy ra phản ứng sau:
SiO2 + 2NaOH = Na2SiO3 + H2O (1)
nếu có mặt Al2O3 sẽ xảy ra phản ứng:
Al2O3 + 2NaOH = 2NaAlO2 + H2O (2)
và có mặt TiO2 sẽ xảy ra phản ứng:
TiO2 + 2NaOH = Na2TiO3 + H2O (3)
Do độ hòa tan của Na2SiO3 và NaAlO2 trong dung dịch kiềm lớn [7] nên khi hòa tan sản phẩm nung, phần lớn SiO2 và Al2O3 hòa tan vào dung dịch và được tách ra khỏi graphit.
Trên thực tế quá trình xảy ra phức tạp hơn nhiều, một mặt là do Si, Al tồn tại ở các dạng khoáng phức tạp nên khi tác dụng với kiềm không tạo thành muối đơn giản như những phản ứng trên, mặt khác cho dù tạo thành các hợp chất natri sili- cat, natri aluminat trong dung dịch chúng sẽ tác dụng với nhau theo phản ứng:
2Na2SiO3 + 2NaAlO2 + 4H2O = Na2O.Al2O3.2SiO2. 2H2O + 4NaOH (4)
Hợp chất natri alumosilicat (Na2O.Al2O3.2SiO2.2H2O) tạo thành sau phản ứng (4) không hòa tan trong dung dịch kiềm. Tuy nhiên, nếu duy trì lượng kiềm lớn sẽ có tương tác:
2Na2SiO3 + 2NaAlO2 + nNaOH → nNa2O.Al2O3.2SiO2. nH2O (5)
và tạo ra natri alumosilicat nhiều kiềm hòa tan rất lớn trong dung dịch kiềm [8]. Như vậy, muốn khử được Si, Al trong giai đoạn này cần phải tiêu tốn một lượng lớn kiềm.
Như vậy, bản chất của công nghệ thường dùng để làm sạch graphit là loại bỏ các tạp chất oxit silic, nhôm ở giai đoạn xử lý với kiềm. Thực tế, các tạp chất sắt, canxi, magie,… không tan trong kiềm nên nằm lại ở pha rắn (chứa graphit). Muốn nâng cao chất lượng graphit, đồng thời với việc loại bỏ các tạp chất này, cần phải tiếp tục xử lý, thông thường chọn phương pháp hòa tách trong dung môi axit.
Như đã trình bày, HCl và H2SO4 là hai dung môi được dùng để khử tạp chất trong quặng tinh graphit. Tuy nhiên, H2SO4 được dùng phổ biến hơn cả. Khi tách tạp chất có trong quặng tinh graphit bằng H2SO4 các phản ứng xảy ra như sau:
Al2O3 + H2SO4 = Al2(SO4)3 + H2O (6)
Fe2O3 + H2SO4 = Fe2(SO4)3 + H2O (7)
CaO + H2SO4 = CaSO4 + H2O (8)
MgO + H2SO4 = MgSO4 + H2O (9)
Quá trình khử tạp chất sẽ tạo thành các muối sunfat tan như: Al2(SO4)3, Fe2(SO4)3, MgSO4 được loại bỏ dưới dạng dung dịch hòa tan và muối CaSO4 không tan sẽ lẫn vào sản phẩm graphit. Do đó, với những quặng tinh graphit chứa hàm lượng canxi cao (> 1 % CaO) thường sử dụng dung môi khác thay vì axit sunfuric nếu yêu cầu sản phẩm graphit chất lượng cao (≥ 99 % C) [5].
Trên cơ sở kết quả thành phần vật chất và tham khảo tài liệu [7], [9], tác giả đã chọn NaOH làm tác nhân nung phân hủy quặng tinh.
Như đã trình bày, sản phẩm phản ứng (4) của quá trình nung không hòa tan trong dung dịch kiềm. Để đánh giá hiệu quả của quá trình nung, sản phẩm sau khi nung phân hủy được đưa đi rửa sạch bằng nước nóng đến pH = 7, tiếp tục hòa tách ở điều kiện chọn trước, cụ thể: dung môi axit H2SO4 nồng độ 10 %, thời gian 1 giờ, tỷ lệ lỏng/rắn = 10, nhiệt độ thường. Sản phẩm cuối cùng được lọc, rửa, sấy khô, cân xác định khối lượng và lấy mẫu phân tích thành phần C. Hiệu suất khử tạp chất (η) được xác định theo công thức:

3.2. Ảnh hưởng của nhiệt độ đến quá trình nung phân hủy
Chế độ khảo sát được lựa chọn như sau [7], [9]:
– Nhiệt độ phân hủy: 300, 350, 400, 450 và 500 oC
– Thời gian phân hủy: 1 giờ
– Chất phân hủy: NaOH
– Tỷ lệ chất phân hủy/quặng tinh: 1/4
Kết quả khảo sát được trình bày trong hình 4.
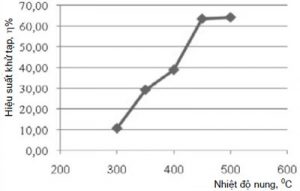
Từ kết quả khảo sát cho thấy, ở nhiệt độ càng cao, hiệu quả phân hủy (đánh giá thông qua hiệu suất khử tạp chất) của NaOH đối với quặng tinh graphit càng tốt. Tuy nhiên, ở nhiệt độ > 450 oC, NaOH không phát huy thêm nhiều khả năng phân hủy mà chi phí năng lượng lại tăng lên. Mặt khác, càng xa nhiệt độ cháy của graphit (~ 800 oC điều kiện thường hoặc 690 oC, 245 torr PO2 hoặc 720 oC, 16 torr PO2) [10], [11] thì sự cháy của graphit càng hạn chế.
Từ đó, chọn nhiệt độ nung phân hủy ở 450 oC.
3.3. Ảnh hưởng của thời gian nung phân hủy
Chế độ khảo sát được lựa chọn như sau [7], [9]:
– Nhiệt độ: 450 oC
– Thời gian: 0,5; 1; 1,5 và 2 giờ
– Chất phân hủy: NaOH
– Tỷ lệ chất phân hủy/quặng tinh: 1/4
Kết quả khảo sát được trình bày trên hình 5.
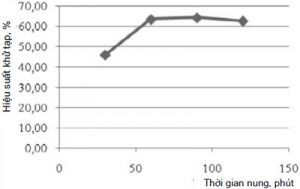
Từ hình 5 ta thấy, thời gian nung càng dài, hiệu quả phân hủy quặng càng tốt. Tuy nhiên, nếu thời gian nung quá dài hiệu quả nung không những không tăng mà lại có xu hướng giảm đi do xảy ra hiện tượng đóng rắn sản phẩm sau nung.
Xét hiệu suất khử tạp chất cũng như hàm lượng cacbon đạt được tại hai thời gian 60 và 90 phút cho thấy, sự chênh lệch giữa 2 thời điểm này không nhiều. Chọn thời gian nung phân hủy là 60 phút.
3.4. Ảnh hưởng của tỷ lệ chất phân hủy/quặng tinh graphit
Chế độ khảo sát được lựa chọn như sau [7], [9]:
– Nhiệt độ phân hủy: 450 oC
– Thời gian phân hủy: 1 giờ
– Chất phân hủy: NaOH
– Tỷ lệ chất phân hủy/quặng tinh: 1, 1/2; 1/3; 1/4 và 1/5.
Kết quả khảo sát được trình bày trên hình 6
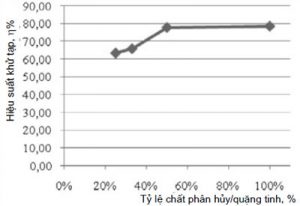
Từ hình 6 ta thấy, tỷ lệ chất phân hủy/quặng tinh càng lớn (hay độ dư NaOH càng lớn), hiệu quả khử tạp chất (chủ yếu là Si và Al) càng cao nhờ tạo thành hợp chất alumosilicat giàu kiềm có độ hòa tan rất lớn trong dung dịch kiềm [7]. Tuy nhiên, độ dư kiềm cao lại gây khó khăn cho quá trình lọc, rửa sản phẩm sau nung phân hủy. Do đó, để vừa đảm bảo hiệu suất khử tạp chất, vừa thuận lợi cho công đoạn xử lý tiếp theo, chọn tỷ lệ chất phân hủy/quặng tinh graphit là 1/2.
3.5. Tổng hợp chế độ nung phân hủy và thử nghiệm tính ổn định công nghệ
Trên cơ sở kết quả thí nghiệm quy mô 100 g quặng tinh graphit/mẻ, đã tổng hợp chế độ nung phân hủy quặng tinh graphit Bảo Hà như sau:
– Chất phân hủy: NaOH
– Nhiệt độ nung: 450 oC;
– Thời gian nung: 1 giờ
– Tỷ lệ chất phân hủy/quặng tinh: 1/2
Đã tiến hành thử nghiệm tính ổn định của công nghệ với quy mô 0,5 kg/mẻ. Kết quả thử nghiệm được trình bày trong bảng 4.
Bảng 4. Kết quả thử nghiệm nung phân hủy quy mô 0,5 kg/mẻ
| STT | Thành phần C, % | η, % |
| TN 1 | 95,65 | >98 |
| TN 2 | 95,71 | >98 |
| TN 3 | 95,49 | >98 |
| TB | 95,62 | >98 |
Từ bảng 4 thấy, sản phẩm trong mỗi thí nghiệm đều đạt > 95 % C, hiệu suất thu hồi > 98 %, tương đương với thí nghiệm quy mô 100 g/mẻ. Điều đó chứng tỏ rằng, chế độ công nghệ đã lựa chọn có tính ổn định.
4. Kết luận
Từ kết quả nghiên cứu thành phần vật chất quặng tinh graphit Bảo Hà, đưa ra một số kết luận sau:
– Bằng các phương pháp phân tích phổ biến hiện nay như: phương pháp hóa học, phương pháp nhiễu xạ tia rơnghen và khoáng tướng, thạch học đã cho thấy, cacbon tồn tại trong quặng graphit Bảo Hà ở khoáng graphit, với hình thù dạng tấm, vảy và một phần rất nhỏ dạng kết tinh vô định hình. Các tạp chất có trong thành phần tro chủ yếu là oxit của silic, nhôm, sắt, canxi, magie có thể loại bỏ bằng phương pháp hóa học.
– Đã khảo sát quá trình nung phân hủy quặng tinh graphit với kiềm nhằm xác định một số yếu tố ảnh hưởng đến quá trình nung phân hủy. Chế độ công nghệ nung phân hủy được lựa chọn như sau: nhiệt độ: 450 oC, thời gian: 1 h, tỷ lệ NaOH/quặng tinh graphit: 1/2.
– Dựa trên chế độ công nghệ nung phân hủy lựa chọn, đã thử nghiệm quy mô 0,5 kg/mẻ nhằm đánh giá độ ổn định của công nghệ. Sản phẩm nhận được cho thành phần C tương đương mẫu thí nghiệm quy mô nhỏ phòng thí nghiệm.
Tài liệu tham khảo
- C. J. Mitchell, Industrial Mineral Laboratory Manual, Flake Graphite, British Geological Survey, 1993
- Wissler, Graphite and carbon powders of electrochemical applications, J. Power Sources, 156, 2006, p 142-1503
- D. N. Lu, Non – Metallic Ore 37(1), China, 1999
- X.W. Yang, Hydrometallurgy, Science Press, Beijing, China, 1996, p. 245
- Y.Z. Lan, S.Zhang and G.Y. Wu, A new process for producing high grade graphite for use in manufacturing Mg-C bricks in steel making, Acta metall. Sin. (Engl. Lett.) Vol. 19 No. 2, Apr 2006, pp 139-143
- Nguyễn Bảo Linh và nnk, Báo cáo tổng kết đề tài cấp cơ sở, Nghiên cứu công nghệ tuyển graphit mỏ Bảo Hà, Lào Cai, Viện Khoa học và Công nghệ Mỏ – Luyện kim, 2014
- Báo cáo tổng kết đề tài “Nghiên cứu công nghệ nâng cao chất lượng graphit” Viện luyện kim màu, 1985
- D. Jozef Formanek, Jaroslav Krizek, Karel Stepan, Khai thác, tuyển, sử dụng graphit trong công nghiệp (Tiếng Tiệp), 1967
- X. J. Lu, Preparation of high – purity and low – sulphur graphite from Woxna fine graphite concentrate by alka- li roasting, Minerals Engineering, 15(10), 10/2002, p 755-757
- A. Gulbransen, K. F. Andrew and F. A. Brassart, The oxidation of graphite at temprature of 600o to 1500oC and at pressures of 2-76 Torr of oxygen, Journal of the electrochemical society, Vol 110 (6), 1963, p 476-483
- J. Tyler, H. J. Wouterlood, M. F. R Mulcahy, Kinetics of the graphite – oxygen reaction near 1000oK, Carbon, Elsevier, Vol 14 (5), 1976, 271-278
